毎回、血と汗と涙の結晶としてできあがるこの化学のこばなし。楽しんで読んでいただけているでしょうか。一所懸命書いても、つまらないときは、「つまらん!お前の話はつまらん!」と言っていただいたほうが、私にとって、今後の勉強になります…。
■感動の銀樹
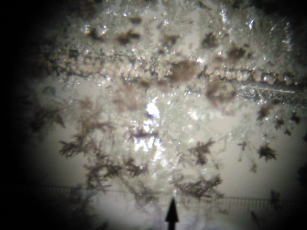
今を去ること1ヶ月前(2003年6月)。私は「大人の化学クラブ」という行事を担当し、参加している皆さんに、いろいろな結晶を作ってもらったり、観察してもらいました。その日の最後の実験として、「銀樹」(写真1)と呼ばれる銀の結晶を顕微鏡を使って見てもらったのですが、参加している皆さんから「きれいですね。」「素敵ですね。」と感動の声が上がりました。
 |
| 写真1.銀樹 |
以前、友の会の例会でも見てもらったことがあるのですが、覚えていらっしゃいますか。
硝酸銀と呼ばれる薬品を水に溶かし、それを銅線にかけると、見ている間にどんどん銀の結晶が出てくるのです。まるで雪山の樹氷のような形で、しかもきらきらと出てくるので「銀樹」と呼ばれています。実際にこの様子を見ると自然のなす業に感動を覚えてしまいます。
この現象は、銀と銅のどちらがイオンになりやすいかを端的に示すものです。銅の持つ電子が、銀イオンに取り込まれ、銅原子は銅イオンに、銀イオンは銀原子になっているのです。
Cu(銅) → Cu2++2e−
Ag++ e− → Ag(銀)
■ 結晶とは
では、結晶とはいったいどんなものをさすのでしょうか。固体はすべて結晶でしょうか。簡単に説明すると、その物質を構成する原子、分子、イオンなどが3次元的に周期的に並んでいるものを結晶と称しています。3次元的な配列の規則性は、結晶格子と呼ばれる立体構造とその対称性で表されます。そして、この規則性が、光学的、電気的な性質も決めるようになります。
具体的にはどんなものをさすのでしょう。一番身近なものでは、塩がありますね。塩、そう塩化ナトリウムです。これはナトリウムイオンと塩化物イオンの繰り返しで作られているものです。
また、鉄、アルミニウムといった金属も結晶になります(表1)。結晶以外のものには、液晶、そしてガラスのような非晶質と呼ばれるものがあります。
表1.結晶の種類
| 結晶の種類 | イオン結晶 | 金属結晶 | 共有結合結晶 | 分子結晶 |
| 主な物質 | 塩化ナトリウム | 鉄・金 | ダイヤモンド | ナフタレン |
| 融点及び沸点 | かなり高い | ばらつく | 非常に高い | 低い |
| 電気伝導度 | 固体にあるが、 液体にない |
かなり高い | なし | なし |
ダイヤは、炭素が立体的に共有結合を取ることで一番硬い物質になります。そして人々を魅了する輝きを放つのですが、結晶構造が変わり、共有結合と分子間力で構成されると真っ黒な炭になってしまいます。ルビーやサファイアも酸化アルミニウムの結晶ですが、含まれている微量元素が違うだけで赤や青の宝石になるのです。ちなみにクロムが入ると赤いルビー、では、青いサファイアには何と何がはいるのでしょう?
 |
| 図2.ルビー(左)とダイヤ |
■結晶の実験はいかが…
最後に、皆さんがご自宅で簡単にできる結晶の実験をご紹介しましょう。用意する薬品は、食塩と消毒用アルコールもしくは燃料用アルコールです。まず、食塩の飽和水溶液を作ります。ちなみに、水100mlに食塩を約30g溶かすと飽和水溶液になります。この食塩水を、細長い透明な容器に入れ、続いてアルコールを食塩水の上に層になるように加えます。すると、食塩水とアルコールの境目あたりから白いものが、サーッと降り注ぐのです。まるで、雲から雪が降ってくるようです。落ちてくるのはもちろん塩の結晶。この実験、簡単にできて、しかも結構見とれてしまいます。実験後はもちろん飲用不可ですが、ぜひ一度お試しあれ。
(2003.8月号うちゅうより)
その他話題トップへ